A. Firma Güvenilirliği:
Çinli firmanın aşılarına ruhsat alabilmek için giriştiği ve yakalanıp yargılandığı rüşvet skandalları ile bezeli hayli karanlık geçmişi ve bugününden hareketle Filipinler’in bile aşı deneyi için etik onay vermediği aşıların deneyine Türkiye en büyük katılımcı sözüyle, Brezilya ve Endonezya’nın yanında gönüllü oluyor.
Çin’de ilaç ve aşı ruhsatlandırması prosesisinin 2001’de merkezileştirilmesi ile birlikte, Çin Gıda ve İlaç İdaresi başkanının 2007’de idamına karar verilmesini gerektirecek ölçü ve sıklıkta rüşvet skandallarının da yolu açılmış oluyor. Türkiye’nin bilim kurulunun tavsiyeleri doğrultusunda Sağlık Bakanlığı tarafından tıp hukuk ve etik ilkeleri çiğnenerek aşısına acil kullanım izni verilen Sinovac’ın bugün insanımız üzerinde denenmekte olan Sars-CoV-2 aşısının teknolojik ve ilmi altyapısını, yepyeni bir firma olarak hemen 2003’teki SARS salgını için geliştirmeye çalıştığı ‘öldürülmüş virüs’ aşısına ve mahkeme kayıtlarından da anlaşılacağı üzere, aşısına ruhsat alabilmek için dönemin ilgili bürokratına 2002’de vermeye başladığı belirtilen rüşvetlere borçluyuz. İlginçtir, rüşveti alan yetkili 10 yıl hapis cezasına çarptırılırken, pandemi öngörüsü hayli yüksek Sinovac’ın bugün de konumunu muhafaza eden ve rüşveti veren kişi olan CEO’su ceza almıyor.
Çin’de toplu ölümlerle ve ilgili ilaç ve aşıların toplatılmasıyla sonuçlanan çeşitli vakalar, Türkiye’de aşı piyasasına hakim konumdaki İngiliz GSK firmasının yakın geçmişte Çin’i boğduğu rüşvetlerle ilgili patlak veren skandallar ve GSK’nın ödemek zorunda kaldığı rekor düzeydeki tazminatların haberlerine internetten rahatlıkla ulaşılabilir.
B. Aşı Güvenilirliği:
En bilindik teknikle hazırlanacak virüs veya bakteri aşılarında dahi 8-10 yıl süren aşı geliştirme sürecinden sonra piyasaya çıkan ürünlerde türlü sorunlar ortaya çıkar, kimi piyasadan toplatılmak zorunda kalırken, Çinli firmanın 2-3 ay içinde geçtiği insan deneylerinin ilk iki fazında topu topu 744 kişi üzerinden toplanan ve tamamen firmanın kontrolünde/insafında olan verilerden hareketle Türkiye, 13 bin kişilik denek sözü ile firmanın aşısına talip olduğunu bildiriyor.
Çinli firmanın Çin virüsü üzerinden hazırladığı aşının 3. faz klinik deneylerinin Türkiye ayağının 15 Nisan 2021 tarihinde tamamlanması beklenirken, aşının ocak ayı itibariyle genel nüfusa önerilmeye başlanmış olması ise, dünya genelinde öldürücülük hızı mevsimsel griple aynı seyreden korona virüs tehdidi için asla göze alınmaması gereken ve hatta skandal olarak nitelendirilebilecek bir karar.
Örnek olarak, dünya genelinde bu “salgın”dan orantısız biçimde kötü etkilenen ve ölümlerin en yoğun görüldüğü ülkelerden ABD’ye uzanıyor ve CDC’nin verdiği CV-19 enfeksiyonundan hayatta kalma oranlarını gösteren resmi istatistiklere bakıyoruz:
| 0-19 yaş için: %99.997 |
| 20-49 yaş için: &99.98 |
| 50-69 yaş için: %99.5 |
| 70 yaş üzerindekiler için: %94.6 |
Çinli firmanın şu ana kadar yürüttüğü 744 kişilik faz 1&2 deneylerinde de, Brezilya, Türkiye ve Endonezya’da yürütülmekte olan faz 3 deneylerinde de aşının sadece 18 – 59 yaş aralığındaki sağlıklı erişkinlerde etkinlik ve güvenlik profilinin çalışıldığı ve henüz çalışmanın da devam ettiği düşünüldüğünde, Türkiye Cumhuriyeti Sağlık Bakanlığı’nın aşıyı bu yaş grubu haricindekilere, altta yatan sağlık sorunu/sorunları olup olmadığı ayırt edilmeksizin önermiş olması tıp etiği ve hukuku bakımından ivedilikle değerlendirilmeli, hiçbir bilimsel veriye dayanmadan verilen bu uygulama kararlarının suç teşkil edip etmediği acilen görüşülmelidir.
TARİHTE YOLCULUK
İnaktif / Öldürülmüş Virüs Aşılarının Skandal ve Felâketlerle Bezeli Tarihsel Güvenilirlik / Tehlike Profili
İPA – İnaktif Salk Polio (çocuk felci) Aşısı
Şimdilerde GBS – Guillain-Barre Sendromu olduğu anlaşılan ABD’nin dönem başkanı Franklin D. Roosevelt’in paralitik durumunun reklam ve bağış kampanyalarının mızrakbaşı yapıldığı 1950’lerde, tarım ilaçlarında kullanılmaya başlanan sinir sistemi zehri ağır metallerin yarattığı felç vakası öbeklenmelerinin virüs kaynaklı olduğu varsayım ve inancı üzerinden aşı geliştirme çalışmaları yarışa dönüşüyor.
Amerikalı mikrobiyolog tıp doktoru Jonas Salk 26 Mart 1953’te polio aşısı geliştirmeyi başardığını duyuruyor ve 1954’te “halk sağlığı” adına tarihin o zamana kadarki en büyük deneyi yapılıyor. Kanada, Finlandiya ve ABD’den anne-babaların adeta birbirini ezerek saha deneyine yazdırdığı 620 binin üzerine “polio öncüsü” çocuğa aşı ve plasebo iğneleri uygulanıyor, bir milyonun üzerinde kişi de kontrol olarak izleme alınıyor. 1 yılı bulmayan saha deneyinin ardından ABD’nin Sağlık, Eğitim-Öğretim ve Sosyal Hizmetler bakanlığı sadece 2 saat süren toplantının ardından Salk’ın aşısını “güvenli ve etkili” bulduğunu söyleyerek onaylıyor.

1955 baharına gelindiğinde, Salk’ın formalin (formaldehid) adlı kimyasal ile “öldürüldüğü” için vücutta çoğalıp felce yol açamayacağı garantisi ile “polio virüsü”nün (esasen maymunlara ait türlü yabancı dokular ve kimyasalların) vücutlarına tanıtıldığı çoğunluğu çocuk olmak üzere 400 binin üzerinde kişinin yarıya yakınında “aşıya bağlı polio paralizisi” gözlemlenmeye başlıyor. 1 aya kalmadan, aşı kampanyasına ara verilmek zorunda kalınıyor.
Sonuç: 70 bin kas güçlüğü, 164 ağır felç, 10 ölüm vakası. Aşı kurbanlarının dörtte üçü (%75’i) ömür boyu felçli kalıyor.
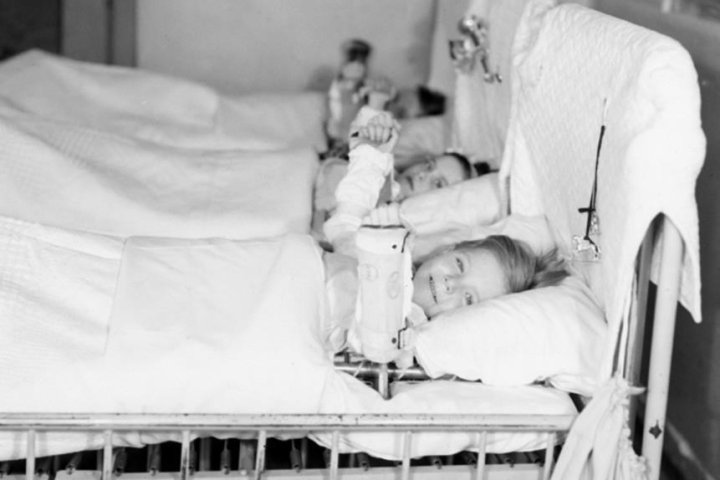
1963’te ABD Salk’ın IPA aşısı yerine, Amerikalı mikrobiyolog ve Salk’ın rakibi Albert Sabin’in ağızdan uygulamalı “zayıflatılmış” virüs aşısını (OPA) kullanıma alıyor. Aşı tarihinin reklamı hiç yapılmayan bir diğer skandalı da işte böyle doğuyor.

YEŞİL MAYMUN BÖBREKLERİ, VİRAL KONTAMİNASYON, KANSER VE AIDS
ABD sağlık bakanlığına bağlı NIH – Milli Sağlık Enstitüleri’nde Salk’ın polio aşı ekibinde güvenlikten sorumlu virolog olarak çalışırken Bernice Eddy, maymunlara vurduğu Salk’ın polio aşısının ağır felce yol açtığını fark eder etmez kurumda üslerine bildiriyor. İdari yetkililer kendilerine delil olarak iletilen felçli maymun fotoğraflarına el koyuyor, Eddy’yi polio takımınından alıp “influenza” (grip) ekibine veriyor ve bu ciddi tehlikeyi bildikleri halde aşıya onay verip çocuk ölümlerine yol açmış oluyorlar.
Eddy 1959’da bu defa da Sabin’in polio aşılarında kansere yol açma kabiliyeti olan enfeksiyöz ajan (SV40 virüsü) tespit ediyor. Durumu üslerine bildirdiğinde bu defa da kamuoyuna açıklama yapma yasağı getiriliyor, laboratuvarı elinden alınarak görevden uzaklaştırılıyor.
1960’da aşı tarihinin iki devi, Merck ilaç firması çalışanı Dr. Maurice Hilleman ve Dr. Benjamin Sweet, virüs üretimi için kullanılan maymun böbreği hücrelerinden karışmış ve o güne kadar fark edilmemiş SV40 maymun virüsünün Sabin’in bütün aşılarında bulunduğunu teyit ediyor. Aşıda bulunmuş 40. maymun virüsü olduğundan ‘simian virus 40’ ismini verdikleri ve insanda kansere yol açtığı bilinen bu virüs, daha sonraki incelemelerde Salk’ın inaktif IPA aşılarında da bulunuyor.
2001’e gelinene kadar kemik, akciğer, hipofiz ve tiroit bezi kanserleri de dahil olmak üzere insan doku ve tümörlerinde SV40’a rastlanmış olduğunu bildiren 58 tıbbi yayın birikmiş oluyor. Dr. Hilleman’ın bir belgesel için yaptığı ve ses kaydı mevcut konuşmasındaki bildirimi, Merck ilaç ve aşı firmasının aşının virüsle kontaminasyonundan haberdar olduğu, buna rağmen çocuğundan yaşlısına kadar tüm popülasyona uygulanmasına devam edildiğini yönünde oluyor.
Amerikan enfeksiyon hastalıkları uzmanlarının bayrak gemisi CDC’nin, kanser virüsü bulaşık aşıları halka verdiğini itiraf etmesi 50 sene alıyor. Sonradan sitesinden silinmesine rağmen yakın geçmişe kadar bu konudaki açıklamalarında ifade, 30 milyon kadar Amerikalının oldukları inaktif ve zayıflatılmış polio aşılarından dolayı kanser riski altında olduğu yönündeydi.
Polio aşısı üretimi için bugün hâlâ maymun böbreği kullanılmakta ve Çinli Sinovac firmasının CoronaVac aşısı için tercihi de aynı. Maymun hâlâ aynı hayvan, bu aşı geliştirme tekniği de belli ki hâlâ vazgeçilmezimizken, Sağlık Bakanlığı’na bağlı görev ifa eden bilim kurulumuza resmi yoldan derhal sorulması gereken sorular şunlar:
- Maymun virüsü bulaş ihtimaline karşı üretici firmanın uygulamak zorunda olduğu yasal protokol nedir?
- Sinovac’ın aşısına Türkiye’den denek sağlama kararı almadan önce bilim kurulu Çinli firmadan ve elbette firmanın bildirimi haricinde aşı örneklerini laboratuvar analizine tabi tutmuş ve aşı içeriğini kontrol etmiş olması gereken Türkiye İlaç ve Tıbbi Cihaz Kurumu’ndan aşıda “Sars-CoV-2 virüsü” haricinde başka herhangi bir yapı bulunmadığı yönünde rapor talep etmiş midir?
- Analiz raporları nerede yayımlanmıştır?
- Maymun virüslerinin yalnız %2 kadarı bilindiğine, yalnız varlığı bilinen şeyin testi yapılabileceğine ve gördüğümüz üzere dünyanın ücra bir köşesindeki yarasadan insan türüne zıplayabilen bir “virüs” bile “ölümcül”(!) olabildiğine göre, çocuklarımıza IPA ve OPA şeklinde en az 4-5 doz uyguladıkları polio aşıları ve bugün tüm popülasyona uygulanmasını öngördükleri Sinovac’ın korona aşılarındaki muhtemel çoklu virüs bulaşını nasıl önlemeyi düşünmektedirler? Sinovac’tan bu konuda ne tür bir güvence alınmıştır, bu konuda bilimsel bir rapor hazırlayıp sunmaları gerekir.
- Polio aşısı üretiminde en çok tercih edilen Afrikalı yeşil maymunların yarıya yakınının “simian immunodeficiency virus (SIV), yani AIDS’e yol açtığı düşünülen insan immünyetmezlik virüsü HIV’nin yakın akrabası olan maymun virüsü ile enfekte olduğu belirtilmekte. Sinovac hangi maymunlardan doku örneği, hücre hattı kullanmıştır, bunların temiz olduğuna dair raporlar kamuoyuyla paylaşılmış mıdır? Aşı takviminin genişlemesi ile birlikte çocuk popülasyonda patlama yaşayan ve otizm teşhisli çocukların primer bulgusu olan immün yetmezlik durumunun, bilim kurullarının önermesi ile maymun dokularından elde edilmiş virüs aşılarının rutin aşı takvimine alınmış olması ile bir alakası olabilir mi?
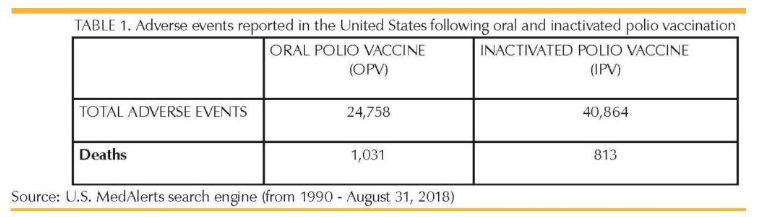
- FDA’ya göre aşıya bağlı olumsuz etkilerinin en fazla 100’de 1’inin sisteme bildiriminin yapıldığı ABD’de 1990’dan 2018’e kadar OPA ve IPA aşılarına bağlı sakatlık ve ölüm rakamları yukarıdaki tabloda görülmekte. ABD’nin 1999 yılında, bizzat paralitik polio’ya yol açtığı için OPA aşısını terk edip ve yalnız IPA uygulamasına yöneldiği, ancak günümüzde Türkiye’de tüm çocuklara (polio eradike edilmiştir denmesine rağmen) her ikisi de hâlâ çoklu kereler uygulanmakta iken, acaba Sağlık Bakanlığı’nın tuttuğu Aşıya Bağlı İstenmeyen Etki Bildirim Sistemi’mizde kayıtlı kaç aşıya bağlı sakatlık ve ölüm vakası bulunmaktadır?
Öldürülmüş / İnaktif Kızamık Aşısı
“Başarılı” polio aşısından sonra bilim camiasının yeni gözdesi kızamık aşısı oluyor. Gerektiğinden değil ama sırf yapılabiliyor diye kızamığın da aşısını yapmaya girişiyorlar. Beklenmedik derecede zorlu çıkıyor iş bu defa; John Enders tarafından ilk geliştirilen ve yumurtada kültürlenen “canlı” aşı Maurice Hilleman’ın tabiriyle “berbat toksik” (toxic like hell) çıkıyor, vurulan çocuklar daha ağır hasta oluyor. “Daha az tehlikeli” olsun, vurulduğu kişide Hilleman’ın tabiriyle nöbet geçirtecek kadar yüksek ateş yapmasın, döküntü çıkmasın diye virüsü formalin (formaldehid) ile “öldürmeye” karar veriyorlar.
Tüm tıp ve bilim camiasının bildiği gibi, formaldehid adlı kimyasal ile etkisiz hale getirildiği düşünülen “virüs” aşısı hem çok kısa “koruma” sağlıyor, hem de literatürde “atipik kızamık” olarak bilinen, yalnız aşılanmış çocuklarda görülen, ağır zatürre tablosu ile karakterize ölümcül “kızamık” enfeksiyonlarına yol açması nedeniyle inaktif virüs aşısının kullanımına son veriliyor.
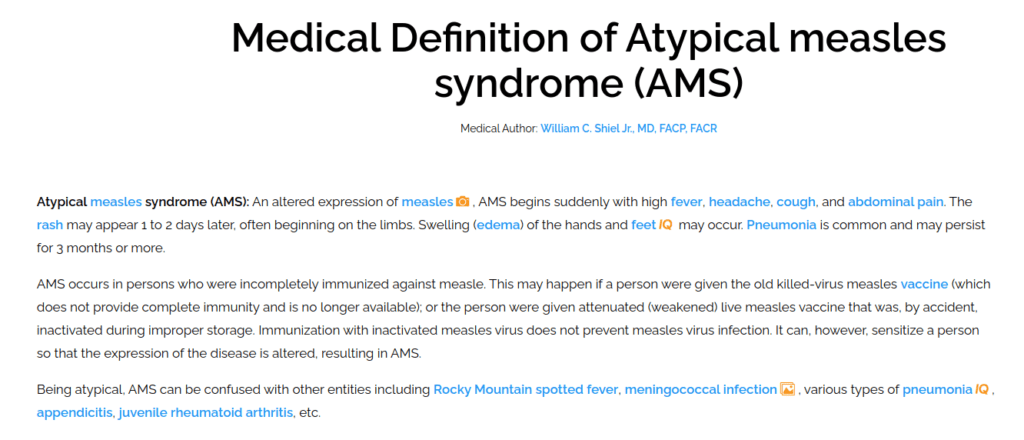
Onun yerine devreye giren “zayıflatılmış” kızamık virüs aşıları daha mı iyi koruyor?
Hayır. CDC 1960 öncesinde doğmuş olup çocukluğunda kendi önerdiği kızamık aşısını olmuş erişkinlere, etkisi çoktan geçmiş olduğu için şu anda yeniden kızamık aşısı önermekte.
Bunun dışında bugün çocuklar 2 doz oldukları karma kızamık aşısını üniversite girişte yeniden olmak zorundalar. Kızamığı doğal yoldan geçirip ömür boyu bağışıklanmalarına izin verilmeyen insanlar, çok ağır yan etkileri olduğu bilinen ve halihazırda inanılmaz kalabalık bir takvimle uygulanan bu aşıları periyodik olarak hayatları boyunca olmak zorundalar artık.
Bunlar dışında bugün kullanımda olan inaktif/öldürülmüş virüs bazlı aşı sayısının ne kadar az olduğu düşünülürse, bu yöntemin ne güvenli ne de etkili bulunduğu aşikardır:
- Hepatit A (iğne şeklinde 2 doz veriliyor)
- İnfluenza (her sene uygulanan ve zaten endüstrinin de pek bir etkinlik beklemediği grip aşısı)
- Japon ensefaliti (iki doz uygulanıyor)
- Polio (çocuklarda ve erişkinlerde 2 doz şeklinde uygulanıyor)
- Kuduz (3 dozluk iğne serisi)
- Tifo (seyahat aşıları arasında, yola çıkılmadan önce tek doz veriliyor)
Aşı deneylerinde Plasebo olarak Alüminyum Kullanımı:
Sinovac’ın Corovac aşı preparatının “güvenlik değerlendirmesi” için yaptığı deneyde, karşılaştırma yapılan plasebonun alüminyum olduğunu görüyoruz.
Bilim kurulu ve sağlık bakanlığının ivedilikle, denenen aşının gerçek tehlike profilinin ortaya çıkmasını engelleyecek, aşıyı olduğundan daha az zararlı göstereceği mutlak olan bu uygulamaya rağmen Corovac’ın neden ve nasıl tercih edilmiş olduğunu açıklamaları gerekir.
Bilim kurulu toplantı tutanaklarından, aşılarda Alüminyum adjuvanının güvenle kullanılabileceğine dair hangi yayınlar esas alınarak karara varılmış olduğu soruşturulmalıdır. Aşılarda alüminyumlu adjuvan kullanımının ile ilgili kısmi bilimsel dokümantasyon için buraya bakınız.
C. Aşı Etkinliği:
Firmanın ve Türkiye’deki yetkililerin “hazır ve güvenilir aşı teknolojisi” olarak lanse ettiği ancak aşı tipleri arasında “koruyucu etkinlik” bakımından en zayıf olduğu bilinen “inaktif aşı” ile kontrol altına alınabilmiş herhangi bir hastalık bugüne kadar olmadığı gibi, korumadaki bu başarısızlık yüzünden inaktif aşı kullanımı gitgide terk edilmiş, kalanların da takvimlere eklenen doz sayısı (etkinsizliğinin kanıtı olarak ve olanca yan etkisi ile birlikte) yıllar içerisinde hep artmıştır.
Günden güne ve kişiden kişiye mutasyona gitme kabiliyetine sahip olduğu öne sürülen bir virüs için geliştirilmiş inaktif aşıda ise bunun herzamanki gibi, aşı korumadıkça ve içindeki kimyasallar ve metaller yüzünden bilakis, insan hastalandırdıkça endüstrinin en sevdiği ve etkin şekilde kullandığı “yeterince kişi aşılanmadığı için sürü bağışıklığı sağlanamadığı, hastalığın o yüzden ara ara patlak verdiği” iddiası üzerinden aşıların koşulsuz şartsız herkese her seferinde çoklu kereler zorla uygulanması sonucuna çıkacaktır.
D. Çelişkili Etkinlik Bildirimleri:
Aşının koruyucu etkinliği ile ilgili deney yürütülen 3 ülkeden birbirinden çok farklı ve hatta kendi içinde revizyona uğramış bildirimlerin gelmesi bilimsel bakımdan büyük soru işaretleri doğurmakta, verilen rakamların daha ziyade politik olduğunu akla getirmektedir.
| BREZİLYA | ENDONEZYA | TÜRKİYE |
| %50,4 Daha sonra %78, fakat sonra yeniden%50 olarak açıklanıyor | %65,3 | %91,25 |
| 12400 kişilik örneklem | 1600 kişilik örneklem | 1322 kişilik örneklem |
| 18 Ocak 2021 | 11 Ocak 2021 | 13 Ocak |
Bu konunun çözümlenmesi ise hiç kolay değil, hatta belki imkansızdır, zira ortada CV-19 enfeksiyonu teşhisinde kullanılan standart klinik bulgu listesi olmadığı gibi, hiçbir güvenilirliği (altın standardı) olmayan ve asla hastalık teşhisinde kullanılmaması gereken ve çıkacak sonucun çok rahat manipüle edilebildiği kanıtlı PCR test sonuçları üzerinden açıklanan “pozitiflik” ve yanlış şekilde bununla eşleştirilen “vaka sayıları” ile olmayan hastalığı da salgın haline getirebilirsiniz, aşınızın etkinliğini de istediğiniz oranda gösterebilirsiniz ve elbette bu iş endüstri için sürekli gelir kaynağı olduğundan “seçeceğiniz hayali herhangi bir hastalığı” istediğiniz süre yaşatabilir, istediğiniz popülasyonda istediğiniz an hortlatabilir, bu kişilerin ısrarla ve zorla aşılanmasını sağlayabilir, sağlıkları ve hayatlarıyla dilediğiniz gibi oynayabilir, politik rakipleriniz ve “istenmeyen gruplar” için bu işi “zorla insan hayatı kurtarma maskesi” altında susturuculu silah olarak kullanabilirsiniz.
E. Aşının Çelişkili / Eksik İçerik Listesi, Yol ortasında Değiştirilen Üretim Tekniği
Aşının Türkiye’den elde edilen ürün bilgisinde üretimde kullanılan kimyasal ve adjuvanların tümünün listelenmemiş olduğu görülmekte (1).
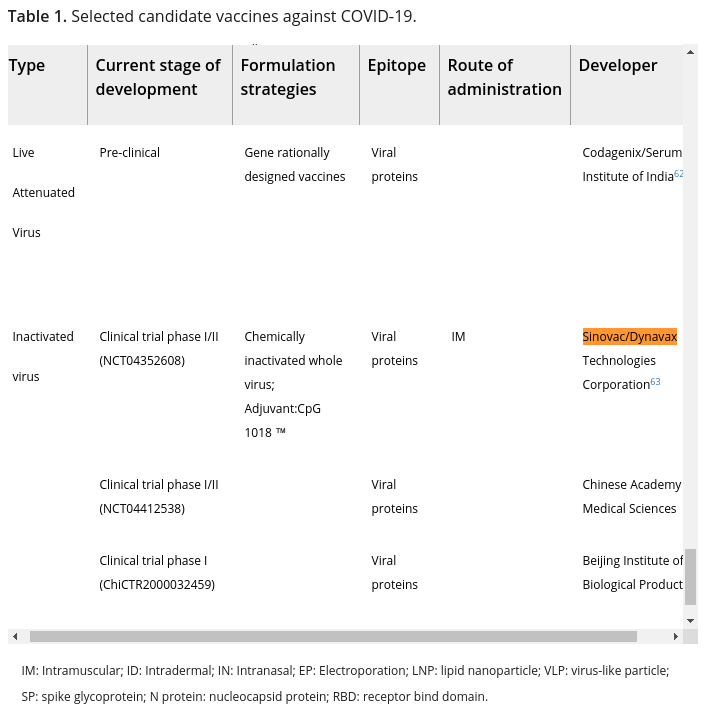

Firmanın Faz 1&2 deneylerine yönelik The Lancet dergisinde yayımladığı makaleden görülebileceği üzere, en eski / en bilindik aşı üretim tekniğidir diye lanse edilmesine rağmen firma klinik deneyler devam ederken üretim kapasitesi artırımı için cihaz değişikliğine gittiğinde tesadüfen, yeni geçilen üretim tekniği ile aşıdaki “virüs”lerin “spike” proteinlerinin daha az bozulmuş olduğunu, bu yüzden de “virüs”ün antijenisite özelliğinin yükseldiğini hayretle görüp bildiriyorlar. Bu teknik konuyu ileride daha ayrıntılı ele alacağız.
“Aşı bilmi”nin en bilindik kompartmanlarına serpiştirilmiş irili ufaklı soru işaretlerini, her iki yöne de çalışabileceği unutulmaması gereken bu “minik sürpriz”leri bir tarafa bırakırsak, firmanın yayınlarını okumuş olanlarımızın anlayabileceği, “bilim kurulu”muzun mutlaka anlamış olması lazım geldiği üzere, toplum geneline uygulanmak üzere seçtikleri aşının ilk 2 faz deneyde sağladığı en yüksek antikor seviyesi bile, CV-19 geçirdiği öne sürülen hastalarda tespit edilen antikor seviyesinin hayli altında kalıyor. Bu da tarihsel olarak öldürülmüş virüs aşılarının sergilediği performansla birebir uyuşuyor.
Acaba bunun nedeni, virüs inaktivasyonunda firmanın tercihi olan betaPropiolactone adlı kimyasalın “virüs” yapısını formaldehidden de beter bozuyor oluşu, bu yüzden de bu kimyasal ile “öldürülen” virüs aşılarında bir türlü istenen “koruyucu etkinlik” seviyelerinin yakalanamıyor oluşu olabilir mi? Bilim kurulumuz bu sorunu cevabını bilecektir diye tahmin ediyoruz.
Bu bilgiler ışığında okurlarımız, yukarıdaki tabloda Türkiye’den bildirimi yapılmış aşı etkinlik değerinin geçerlilik ve güvenilirliği ile ilgili akıllarına gelmiş olabilecek soruları Sağlık Bakanlığı bünyesinde hizmet veren bilim kurulu üyelerine resmi yoldan sormak isteyebilirler.
Bizim aklımıza gelen etkinlikle ilgili sorular şu şekilde:
- Firma, CV-19 tanı kriterleri de, “virüs tespiti” için kullanılan PCR cihazları da, bu cihazlara tanımlı virüs gen dizilimleri de, kullanılan devir sayıları da, ülkeden ülkeye görüldüğü ileri sürülen virüs alttipi de bambaşka birkaç ülkeden, CV-19’luydu denilen kişilerden salgı örnekleri alıyor ve sonunda yine gidip Çinli bir hastanın salgısını kullanıyor.
Bilim kurulu üyeleri firmadan virüs izolasyonunun nasıl gerçekleştirilmiş olduğunu, virüsün morfolojik tanımlamasını, genetik dizilimini, spike protein yapısını ihtiva eden belgeleri talep etmiş, gerekli incelemeleri yapmış, bu “virüs”ün Türkiye genelinde görülen ancak hızla mutasyona uğradığı söylenen virüs alttipleriyle benzerliği (dolayısıyla aşının “koruma potansiyeli”) konusunda bir çalışma yapmış mıdır? - Türkiye aşı prospektüsünde yazmayan içerik maddelerinin ne olduğuna dair firmadan bilgilendirme istemiş, aşı örneklerini analiz etmiş ve içerikteki maddelerin firmanın belirttiği miktarlarda olup olmadığını, dışarıdan herhangi bir bulaş olup olmadığını kontrol etmiş midir? Evetse, raporlara nereden ulaşılabilinir?
- Mutasyon sorunu nedeniyle aşı kullanımının mantığı zaten büyük soru işareti taşır, firmanın tesadüfen antijenisite yükselten tekniği keşfetmiş olmasına rağmen aşısıyla kanda sağlayabildiği antikor oranı hastalığı geçirmiş ve olağanüstü sağlık sorunları yoksa istatistiklerin de gösterdiği gibi gayet rahat atlatmış bireylerin kanındaki antikor oranını yakalayamıyor olmasını, risk/fayda dengesi bakımından nasıl değerlendirmişlerdir?
- Lancet yayınından görülebileceği üzere firma faz 1&2 deneylerinde yalnız antikor yanıtına bakmış, aşının T hücresi bağışıklığı oluşturup oluşturmadığına bakmamış. Şu anki tıp paradigmasında enfeksiyonel bir hastalıkta EN ÖNEMLİ parametre, kişide uzun vadeli bağışıklık oluşup oluşmadığını anlamamızı sağlayacak veri eksik, kendi yaptığı ve aşının etkinliğini ortaya koyacak 3. faz klinik deneyin bile Nisan 2021’de bitmesi beklenirken, hakkında elle tutulur hiçbir veri olmayan, yan etki profili de bilinmeyen bu toksik materyalin genel topluma verilmesini bilim kurulu nasıl önerebilmiş, sağlık bakanlığı nasıl onaylayabilmiştir?
- Firmanın Türkiye’ye sağladığı ürün bilgilendirmesinde ismi dahi geçmeyen inaktivasyon ajanının endüstride “en az işe yarayan ve virüsün fiziksel yapısını bozan kimyasal” olarak biliniyor olması, üstelik insanda muhtemel kanserojen etkisinin de bildirilmiş olmasına rağmen mi Bilim Kurulu üyeleri ve Sağlık Bakanlığı bu aşıda karar kılmıştır?
F. Sağlıklı Kişiler Üzerinde Denenmekte Olan Aşının Toplum Genelinde Sergileyeceği Gerçek Emniyet Profilini Bilmek Mümkün Değil

Sinovac’a ait CoronaVac aşısının Türkiye’deki “gönüllüler” üzerinde devam etmekte olan ve 15 Nisan 2021 itibarıyla sonlanması beklenen 3. faz klinik deneyine, yukarıdaki fotoğraftan da görülebileceği üzere 18-59 yaş arasındaki “sağlıklı kişiler” kabul edilmekte.
Bildiğimiz gibi hayli güçlü etkileri bulunan aşı ürünlerinin deneylerinde istenmeyen etki yaşanma ihtimalini azaltmak için firmalar oldukça sağlıklı bireyleri denek olarak kullanmayı tercih etmekte, oysa bu veriler üzerinden ruhsatlandırılan ürünler daha sonra her yaştan ve sağlık durumundan insana aynı doz ve sıklıkta uygulanmakta ve işte ancak o zaman aşının gerçek tehlike profili anlaşılabilmekte, ancak endüstri ile sıkı iş ilişkisi içindeki resmi birimler gerekli yan etki takibini yapmadığından, aşılarla ilgili problemler hiçbir zaman gün yüzüne çıkmamaktadır.
Sinovac aşısının Türkiye’de yürütülen 13 bin kişilik deneyine kimler alınmıyor diye bakacak olursak:
- PCR ile önceden COVID-19 pozitif çıkanlar
- IgG veya IgM pozitif olanlar (yani virüsle önceden temas edip immün yanıt oluşturduğu tespit edilenler)
- Kadın deneklerde: beta-hCG testi ile gebeliği teyitli olanlar, emzirmekte olanlar yahut aşılamayı takip eden 3 ay içerisinde doğum kontrol yöntemi kullanmadan çocuk sahibi omak maksadıyla cinsel ilişkide bulunmayı düşünenler
- Denenmekte olan aşı veya “plasebo” içeriğindeki maddelere alerjisi olanlar (Not: Bunun bilinebilmesi için aşının ve plasebonun tam içeriğinin bilinmesi gerekir oysa sağlanan Türkçe ürün bilgisinde aşı virüsünün hangi kimyasalla deaktivasyonunun yapıldığı dahi yazmıyor, eksipiyan listesi yok, aşıda aluminyum dışında bir adjuvan kullanılıp kullanılmadığı belirsiz. Ürünün ve plasebosunun acilen bağımsız laboratuvarlarda analizi gerekir.)
- Deneye katılmadan önceki 6 ay içinde yahut deney bitiminden sonraki 2 yıl içinde bağışıklık baskılayıcı terapi görmüş veya görecek olanlar.
- İmmünosüpresan terapiler şu şekilde tanımlanmış: antineoplastik kemoterapi, radyasyon terapisi ve nakli gerçekleştirilen organa tolerans ve diğer şeyler için verilen bağışıklık sistemi baskılayıcı ilaç kullanımı
- Deneye katılım öncesindeki 3 ay içinde bağışıklık baskılayıcı dozlarda kortikosteroid ilaç kullanımı olmuş veya deneyden sonraki 3 ay içinde bağışıklık baskılayıcı dozlarda kortikoid ilaçlar kullanacak olanlar.
- Kortikosteroid ilaçlar için bağışıklık baskılayıcı dozlar şu şekilde tanımlanmış: erişkinler için bir haftanın üzerinde günde 20 mg prednisone kullanımı. Topikal veya nazal kortikosteroidler bağışıklık baskılayıcı kabul edilmiyormuş.
- Aspleni öykülüler, yani dalağı olmayanlar.
- Kanama bozukluğu (örn. faktör eksikliği, pıhtılaşma bozukluğu (koagülopati) ceya platelet bozukluğu) öyküsü olanlar veya daha önceki kas içi enjeksiyonlarda yahut kan aldırırken kapsamlı kanama ya da morluk oluşumu yaşayanlar.
- Deneye katılmadan önceki 12 aylık süreçte klinik öykü itibariyle tıbbi, ailevi problemlere veya işyerinde sorun yaşanmasına neden olacak boyutta alkol veya uyuşturucu alımı olanlar
- Aşı vurulma tarihinden önceki 3 ay içerisinde immünoglobülin ve/veya herhangi bir kan ürünü almış olanlar.
- Bu deneye katılmadan önceki 6 ay içinde ilaç/aşı deneyen başka bir deneye katılmış olanlar veya bu deneyden sonraki 2 yıl içinde bir başka deneye katılacak olanlar.
- Deneye katılamdan önceki 14 gün içinde zayıflatılmış bir virüs aşısı olmuş olanlar
- Deneye katılmadan önceki 7 gün içinde inaktif / öldürülmüş tipte aşı veya subünit aşısı olmuş olanlar
- Denenecek aşıyı olmadan önceki 24 saat içinde ateşlenme yaşayanlar (ağızdan ölçümde 37.2℃’ı geçen ateş kastedilmekte, koltukaltı ölçümü kabul edilmiyormuş)
- Deneyi yürüten yetkili yahut kişinin kendi doktoru tarafından deneye katılımının şahsın sağlığı ve hakları bakımından uygun olmadığına veyahut da deneyi kurallarına uygun götüremeyeceğine karar verilenler
- İnsan immünyetmezlik virüsü (HIV) enfeksiyonu da dahil olmak üzere, immünyetmezlik veya otoimmün herhangi bir hastalık tanısı veya hastalık şüphesi bulunanlar
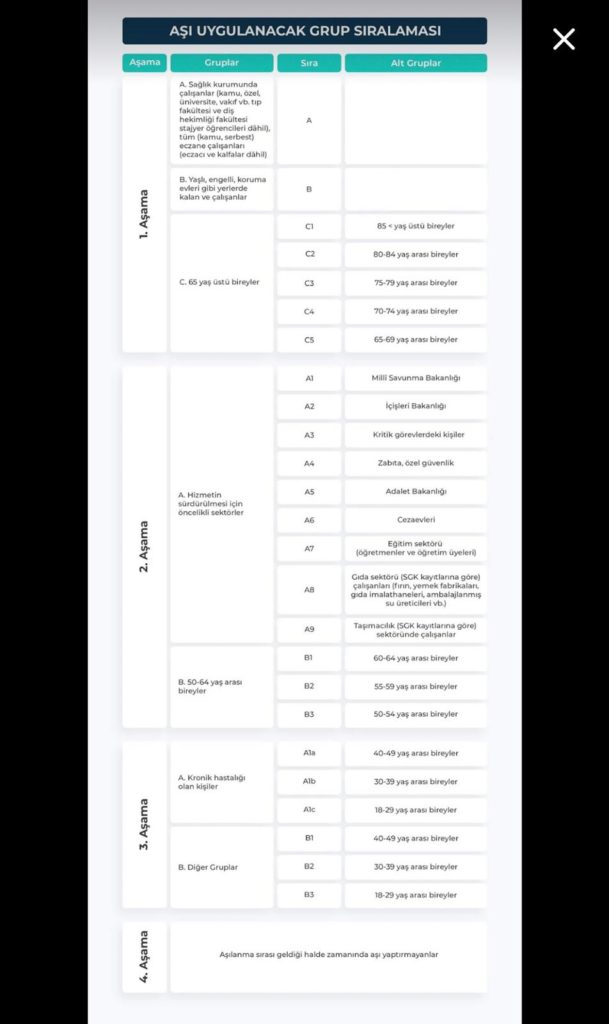
Hâl böyleyken, Bilim Kurulu’nun tavsiyesi doğrultusunda şu anda Sağlık Bakanlığı bu deneysel aşıyı öncelikli olarak yaşlı, engelli, koruma evleri gibi yerlerde kalanlara ve 85 yaş üstü bireylere öneriyor. (2)
Sağlık Bakanlığı’nın toplumda yaş gruplarına göre CV-19 olduğu iddia edilen enfeksiyonu geçirme ve sağ kalım istatistiklerini yayımlaması ve daha deneyleri tamamlanmadan etkinliği ve tehlike profili bilinmeyen bu aşı girişimine “acil” gereksinimi net bir şekilde ortaya koyabilmesi gerekir.
E-nabız sisteminden, isme özel vurulan bu aşıları alanların sağlık geçmişlerini, halihazırda altta yatan ne gibi rahatsızlıkları olduğunu, görmekte oldukları tedavileri, kullandıkları ilaçların dökümünü Sağlık Bakanlığı’nın derhal yayımlaması, aşı uygulaması ardından başgöstermiş hertürlü sağlık sorununu haftalık olarak raporlaması gerekir.
Bu deneysel ancak kişilere bağışıklık oluşturacağı ve hastalıktan koruyacağı yönlendirmesi(3) ile vurulan aşıdan ötürü oluşacak hertürlü yan etkide devletin vatandaşına tazminat ödemesi gerekmektedir.
KAYNAKÇA
(1)


(2)
(3)



